Sciences de la vie & Santé
Mettons la science
au service de la vie
Une demande commerciale ?
Vous souhaitez nous rejoindre ?

Qu’il s’agisse d’investir dans le développement de médicaments et de vaccins pour lutter contre les pandémies mondiales, de développer des technologies de pointe pour améliorer les possibilités de recherche ou de faire face à un environnement réglementé en constante évolution, l’industrie des sciences de la vie se transforme, s’adapte et innove en permanence.
L’industrie des Sciences de la Vie et de la Santé regroupe des entreprises qui se consacrent à la création de produits et de solutions dont l’objectif est d’améliorer la vie des organismes. Ces entreprises agissent dans de nombreux domaines tels que les produits pharmaceutiques, la biotechnologie, les dispositifs médicaux, les technologies biomédicales, les compléments alimentaires, les cosméceutiques, la transformation des aliments, etc.
Bien qu’elle soit l’une des industries les plus réglementées au monde, l’industrie des sciences de la vie reste l’une des plus attrayantes. Le marché global est en croissance constante en raison de l’augmentation de la population mondiale, de l’accès à la médecine dans les pays en développement, du vieillissement de la population dans les pays développés et, circonstanciellement, des demandes liées aux pandémies mondiales sur la santé publique.
L’impact des crises sanitaires mondiales
Si les ralentissements économiques sont inévitables, le secteur des sciences de la vie a connu un changement de paradigme sous l’effet de la pandémie mondiale : collaboration mondiale en matière de R&D, relocalisation stratégique du développement et de la fabrication des produits ainsi que la facilitation réglementaire spécifique et réactive d’une prévention systémique et coordonnée.
Les nouveaux processus récemment développés et utilisés pour lutter contre la pandémie de COVID-19, sont maintenant employés dans la recherche et le développement de nouveaux médicaments et produits thérapeutiques grâce à des essais cliniques plus efficaces. Parallèlement, l’industrie a suscité un intérêt et des investissements considérables dans de nombreux projets innovants, tels que les nouveaux processus numérisés visant à améliorer les performances de production et les usines intelligentes.


ALTEN : Inciter l’innovation dans l’industrie des sciences de la vie
Les futurs leaders de l’industrie des Sciences de la Vie seront ceux qui s’adapteront aux changements, ceux qui auront une vision claire, qui seront prêts à saisir les nouvelles opportunités et à relever les défis, qui établiront des collaborations au-delà des acteurs traditionnels et qui rechercheront les meilleures ressources et les meilleurs partenaires disponibles sur le marché.
ALTEN, leader européen du conseil dans le domaine des Sciences de la Vie, accompagne ses clients dans le développement et la fabrication des produits liés aux Sciences de la Vie et à la Santé autour de 2 grands domaines d’expertise :
- Services d’externalisation de la recherche clinique (CRO)
- Opérations de fabrication dans le domaine des Sciences de la Vie (LSMO)
ALTEN dans l’industrie des sciences de la vie
338 M€
chiffre d’affaires en 2023
+3 000
consultants
25
pays
6
domaines d’expertise :
Industrie pharmaceutique, biotechnologie, chimie, cosmétique, agroalimentaire, dispositifs médicaux
Tendances du marché
Confrontées à des réglementations nouvelles et changeantes, les industries pharmaceutiques et dispositifs médicaux ont l’obligation de s’y conformer.
Par exemple, la mise en œuvre de la Directive européenne sur les médicaments falsifiés, initiée en 2018 , permettra entre 2026 pour les dispositifs implantables sur mesure de classe III et 2028 pour tous les autres dispositifs, dans la plupart des 28 États membres de l’UE, de suivre et d’identifier chaque boîte de médicament à l’aide d’un numéro de série unique. Ce numéro, représenté par un QR code imprimé sur l’emballage du produit, est enregistré dans une base de données de l’Union Européenne et est vérifié par le pharmacien avant que le médicament ne soit administré au patient, éliminant ainsi tout risque de contrefaçon.
Défis :
- Qualifier et valider les systèmes de production et de distribution impactés
- Maîtriser les questions réglementaires liées à l’émergence des produits combinés
- Anticiper les besoins futurs potentiels tels que l’agrégation
- Modifier et mettre à jour les processus et systèmes existants pour assurer la conformité réglementaire.
Tous les dispositifs médicaux sont potentiellement connectables. Certains sont déjà connectés et fonctionnent grâce à des applications proposant aux professionnels de santé et aux patients des aides à la décision, des possibilités de diagnostic ou de gestion de traitement automatique. Les domaines d’application sont nombreux, entre autres la télémédecine, la gestion de la dépendance ou le traitement des maladies chroniques.
Le marché de la e-santé, qui affiche un taux de croissance supérieur à 10% par an, a dépassé les 400 milliards de dollars en 2022.
Défis :
- Développer ces logiciels embarqués conformément aux standards réglementaires du marché concerné
- Prouver la conformité réglementaire de ces produits, doublement complexifiée par les impératifs liés au statut de DM (Dispositif Médical) et par la présence d’un logiciel
- Assurer la sécurité des données personnelles et la confiance des acteurs
Un produit combiné est un produit de santé dans lequel on associe un médicament et un dispositif médical. A l’instar du logiciel embarqué, l’innovation et les progrès techniques permettent de plus en plus ce type d’alliance, et là encore les domaines d’application sont nombreux. On peut citer une association devenue courante, celle de la prothèse de hanche et de l’antibiotique, qui a pour but d’inhiber l’adhérence bactérienne.
La complexité pour les industriels vient du fait que ces produits « frontières » n’ont qu’un seul statut, Médicament ou DM, et que chaque statut a son régime réglementaire particulier. Ici la stratégie réglementaire est prépondérante, dès les phases de conception.
Défis :
- Maîtriser à la fois les contraintes normatives des DM et celles des médicaments, pour développer un produit combiné enregistrable
- Valider le procédé de fabrication de ces produits combinés
- Être capable de qualifier et classifier le produit combiné afin de déterminer le statut réglementaire applicable, et en déposer l’enregistrement
Les industries pharmaceutiques doivent produire davantage à coût compétitif afin de répondre aux efforts budgétaires demandés par les systèmes de santé, à la concurrence accrue des médicaments génériques et à la demande croissante des pays émergents.
En 2017, le marché mondial du médicament a dépassé le seuil des 1 000 milliards de dollars de chiffre d’affaires, en croissance de 6 % par rapport à 2016, avec une part de marché des Etats-Unis de 49%.
Défis :
- Mutualiser les investissements R&D
- Moderniser les outils de production (ex. automatisation)
- Qualifier et valider à nouveau ces sites de production
Valeur ajoutée d’ALTEN
Les secteurs fonctionnels couverts par ALTEN
- Opérations cliniques
- Analyse de données
- Qualité clinique
- Vigilance et information médicale
- Réglementation et autorisation de marché
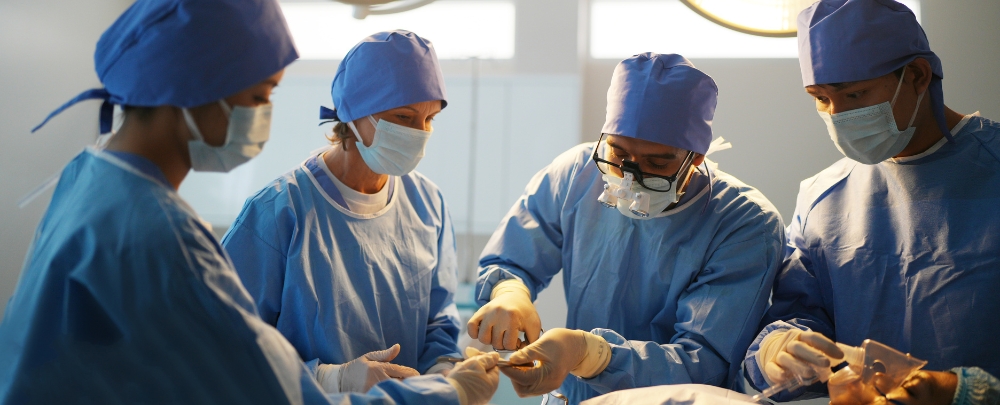
- Fabrication (production, conditionnement)
- Chaîne d’approvisionnement, logistique et achats
- Industrie 4.0
- Lean 6/Sigma et amélioration continue

- R&D
- Transfert de technologie, NPI, NPD
- Ingénierie (maintenance et mise en service)
- Validation (Q&V, CSV, V&V)
- Ingénierie 4.0
- PMO, PM

- Affaires réglementaires
- Assurance qualité
- Contrôle de la qualité
- Qualité 4.0

NOS SUCCESS STORIES
Afin de pouvoir lancer les essais cliniques à grande échelle (phase 3) d’un nouveau vaccin, l’un des dix géants de l’industrie pharmaceutique mondiale a investi en Belgique dans la construction d’un nouveau site de production. ALTEN se voit confier la responsabilité de la qualifier la performance des équipements (PQ) de rédiger les instructions opératoires.
Dans le contexte du développement d’un immunosuppresseur destiné à des patients ayant subi une greffe du rein, un leader mondial des médicaments génériques et biosimilaires a confié à AIXIAL (filiale spécialisée du Groupe ALTEN) la mission de réaliser un essai clinique complet afin de présenter les avantages du profil pharmacocinétique de son produit.
ALTEN dispose d’un savoir-faire reconnu dans les dispositifs médicaux et a mis en place deux centres de service (Software et Hardware) pour accompagner les activités du centre R&D d’un des leaders mondiaux de l’imagerie médicale. Les travaux réalisés par nos ingénieurs s’inscrivent dans les domaines de la mammographie, de la radiologie interventionnelle et du développement d’applications avancées en imagerie médicale.
L’utilisation croissante des technologies numériques dans les industries pharmaceutiques rend notamment nécessaire la validation des systèmes informatiques (CSV, Computer System Validation) qui pilotent la production automatisée des médicaments. Cette validation permet de fournir la preuve documentée qu’un logiciel ou qu’un système informatisé fonctionnera de manière constante et répondra dès lors aux directives GxP (Good Practice) prédéfinies.
Nos clients
Industrie pharmaceutique
Pfizer, Abbvie, Sanofi, Johnson & Johnson, Novartis, GSK, Lonza
Biotechnologie
Novo Nordisk, Moderna, Thermo Fisher, Gilead, Amgen
Cosmétiques
Pierre FABRE, L’OREAL
Agroalimentaire
Syngenta, Danone
Industrie des dispositifs médicaux
Abbott, Siemens Healthineers, Roche, Becton Dickinson et BioMerieux